- Autors Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:45.
- Pēdējoreiz modificēts 2025-01-23 11:14.
Galvenā atšķirība - alifātiskie un aromātiskie ogļūdeņraži
Vispirms īsi apskatīsim, kādi ogļūdeņraži apspriež atšķirību starp alifātiskajiem un aromātiskajiem ogļūdeņražiem. Ogļūdeņraži ir organiskie savienojumi, kuru struktūrā ir oglekļa un ūdeņraža atomi. Galvenā atšķirība starp alifātiskajiem un aromātiskajiem ogļūdeņražiem ir tā, ka alifātiskie ogļūdeņraži nesatur konjugētu saišu sistēmu, savukārt aromātiskie ogļūdeņraži satur konjugētu saišu sistēmu. Tomēr abas šīs molekulas tiek uzskatītas par organiskiem savienojumiem.
Kas ir alifātiskie ogļūdeņraži?
Alifātiskie ogļūdeņraži ir organiskās molekulas, kuru struktūrā ir oglekļa (C) un ūdeņraža (H) atomi; taisnās ķēdēs, sazarotās ķēdēs vai nearomātiskos gredzenos. Alifātiskos ogļūdeņražus var iedalīt trīs galvenajās grupās; alkāni, alkēni un alkīni.
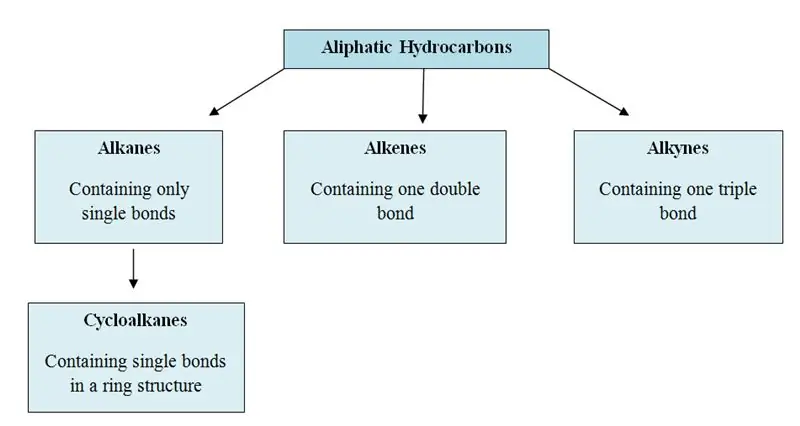
Kas ir aromātiskie ogļūdeņraži?
Aromātiskie ogļūdeņraži dažkārt ir zināmi kā “arēni” vai “arilogļūdeņraži”. Lielākā daļa aromātisko ogļūdeņražu savā struktūrā satur benzola gredzenu; bet ir nebenzola aromātiskie ogļūdeņraži, ko sauc par heteroarēniem un kuri ievēro “Hakla likumu” (cikliskajos gredzenos, kas atbilst Hakla likumam, ir 4n+2 π-elektronu skaits; kur n=0, 1, 2, 3, 4, 5, 6). Dažiem aromātiskajiem ogļūdeņražiem ir vairāk nekā viens gredzens; tos sauc par policikliskajiem aromātiskajiem ogļūdeņražiem.
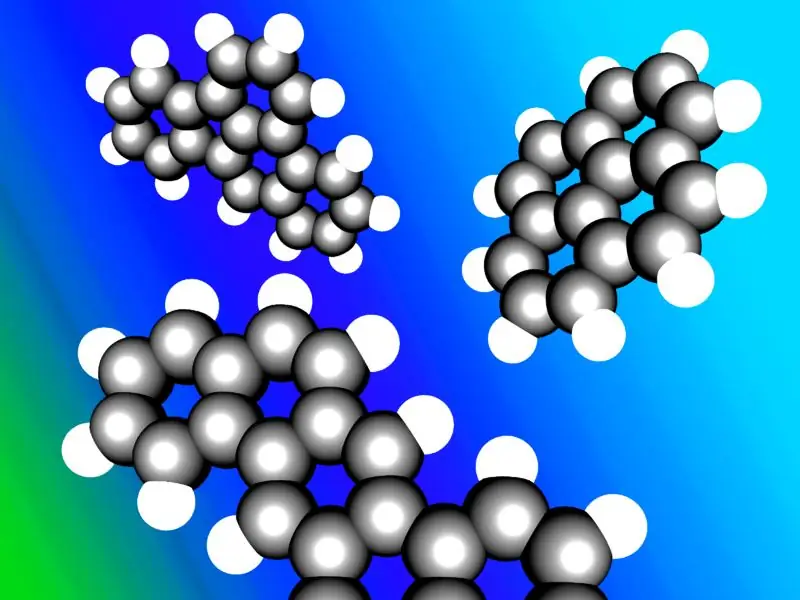
Tipisku policiklisko aromātisko ogļūdeņražu ilustrācija.
Kāda ir atšķirība starp alifātiskajiem un aromātiskajiem ogļūdeņražiem?
Alifātisko un aromātisko ogļūdeņražu struktūra
Alifātiskie ogļūdeņraži: to struktūrā ir taisnas ķēdes, sazarotas ķēdes vai nearomātiski gredzeni. Šajā grupā ir gan piesātinātie, gan nepiesātinātie ogļūdeņraži. Alkāni ir piesātināti ogļūdeņraži, alkēni un alkīni ir nepiesātināti ogļūdeņraži.
Taisnas ķēdes:
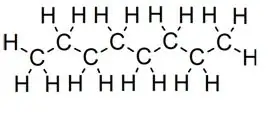
Oktānskaitlis
Zīmola ķēdes:
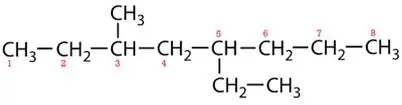
5-etil-3-metiloktāns

2-metil-3-pentence
Nearomātiskie gredzeni:
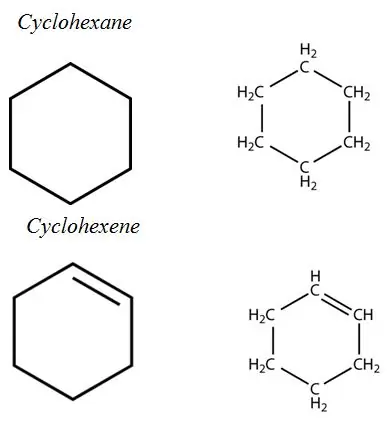
Aromātiskie ogļūdeņraži: aromātisko ogļūdeņražu struktūrā ir aromātisko gredzenu sistēma. Tie visi ir nepiesātināti ogļūdeņraži, taču tie ir samērā stabili konjugēto saišu sistēmas dēļ.
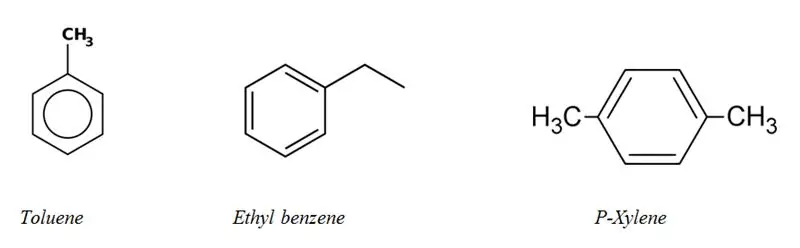
Alifātisko un aromātisko ogļūdeņražu kategorijas
Alifātiskie ogļūdeņraži:
Alifātiskajos ogļūdeņražos ir trīs galvenās grupas; alkāni, alkēni un alkīni. Tos sauc arī par alilogļūdeņražiem.
Alkāni: alkānos oglekļa un ūdeņraža atomi ir savstarpēji saistīti ar atsevišķām saitēm. Viņiem nav vairāku obligāciju. Alkāni veido gredzenveida struktūras, tos sauc par cikloalkāniem.
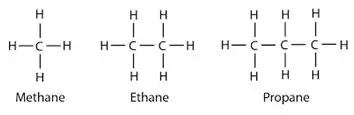
Alkēni: šī grupa satur gan vienas, gan dubultās saites starp oglekļa atomiem. Ūdeņraža un oglekļa atomi vienmēr veido atsevišķas saites.
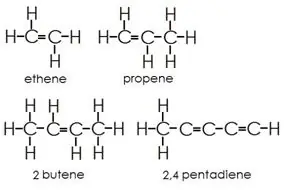
Alkīni: alkīniem ir trīskāršās saites starp oglekļa atomiem papildus vienvietīgām saitēm.
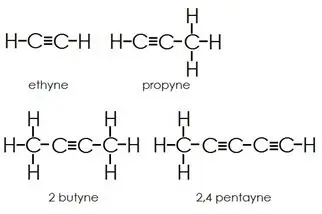
Aromātiskie ogļūdeņraži:
Lielākā daļa aromātisko ogļūdeņražu struktūrā satur vismaz vienu benzola gredzenu. Bet ir maz aromātisko ogļūdeņražu, kas nav benzols, tos sauc par "heteroarēniem". Aromātiskie ogļūdeņraži tiek saukti par “aril” ogļūdeņražiem.
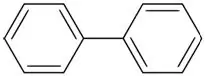
Bifenils (aromātisks ogļūdeņradis ar diviem benzola gredzeniem)
Alifātisko un aromātisko ogļūdeņražu savienošanas modelis
Alifātiskie ogļūdeņraži:
Alifātiskajos ogļūdeņražos; vienkāršās, dubultās vai trīskāršās saites var pastāvēt jebkur molekulā. Dažreiz vienai molekulārajai formulai var būt vairākas struktūras, mainot vairāku saišu(-u) pozīciju. Šīm molekulām ir lokalizēta elektronu sistēma.
Aromātiskie ogļūdeņraži:
Aromātiskajos ogļūdeņražos tiem ir alternatīva vienas un dubultās saites sistēma, lai izveidotu konjugētu saišu sistēmu, lai delokalizētu dažus elektronus. (Delokalizēti elektroni var pārvietoties no vienas saites uz otru).
Alifātisko un aromātisko ogļūdeņražu reakcijas
Alifātiskie ogļūdeņraži:
Piesātinātie ogļūdeņraži tiek pakļauti aizvietošanas reakcijai; nepiesātinātie ogļūdeņraži iegūst stabilitāti pievienošanas reakcijā. Tomēr dažas reakcijas notiek kontrolētos apstākļos, nepārraujot vairākas saites.
Aromātiskie ogļūdeņraži:
Aromātiskie ogļūdeņraži ir nepiesātināti, bet tiem ir stabila konjugēta elektronu sistēma, tāpēc tie ir vairāk pakļauti aizvietošanas reakcijām, nevis pievienošanās reakcijām.
Attēls: Inductiveload “Polycyclic Aromatic Hydrocarbons” - augšupielādētāja, Accelrys DS Visualizer, darbs. (publiskais domēns), izmantojot Commons






